Tentativas de se Isolar o princípio ativo!
 Em 1855, a Sociedade Farmacêutica de Paris ofereceu um prêmio para o primeiro cientista capaz de isolar o princípio ativo da Cannabis sativa. O contemplado foi J. Personee (J. Pharm. Chim. 1855, 28, 461–463), um químico francês. Nem um mês se passou para que a comunidade científica da época constatasse o equívoco: o óleo extraído por Personee não era ativo! Não continha nenhum componente com atividade fisiológica - ao contrário da cannabis. Foi Vignolo, um químico italiano, que descobriu o erro: o óleo de Personee era rico em sesquiterpenos, substâncias abundantes na cannabis, mas sem atividade biológica. Durante várias décadas, a busca pelo princípio ativo da cannabis continuou, em todo o mundo. Enquanto que a morfina, a cocaína, a strychnina, a cafeína e outros alcalóides eram isolados e caracterizados, nenhuma novidade aconteceu com a cannabis. Isto porque, ao contrário dos alcalóides - que são facilmente isolados na forma de sais - os terpenóides (tal como o THC) requerem técnicas químicas mais apuradas, inexistentes até 80 anos atrás. O primeiro químico a obter um extrato ativo da cannabis foi Wood, em 1896, na Cambridge University (J. Chem. Soc. 1899, 75, 20-36). Segundo palavras do próprio autor: "The red oil, is extremely active, and taken in doses of 0.05 g induces decided intoxication followed by sleep. The symptoms produced by it are peculiar to Cannabis indica, and as none of the other products appear to possess this action, this substance must be regarded as the active constituent of the plant."
Em 1855, a Sociedade Farmacêutica de Paris ofereceu um prêmio para o primeiro cientista capaz de isolar o princípio ativo da Cannabis sativa. O contemplado foi J. Personee (J. Pharm. Chim. 1855, 28, 461–463), um químico francês. Nem um mês se passou para que a comunidade científica da época constatasse o equívoco: o óleo extraído por Personee não era ativo! Não continha nenhum componente com atividade fisiológica - ao contrário da cannabis. Foi Vignolo, um químico italiano, que descobriu o erro: o óleo de Personee era rico em sesquiterpenos, substâncias abundantes na cannabis, mas sem atividade biológica. Durante várias décadas, a busca pelo princípio ativo da cannabis continuou, em todo o mundo. Enquanto que a morfina, a cocaína, a strychnina, a cafeína e outros alcalóides eram isolados e caracterizados, nenhuma novidade aconteceu com a cannabis. Isto porque, ao contrário dos alcalóides - que são facilmente isolados na forma de sais - os terpenóides (tal como o THC) requerem técnicas químicas mais apuradas, inexistentes até 80 anos atrás. O primeiro químico a obter um extrato ativo da cannabis foi Wood, em 1896, na Cambridge University (J. Chem. Soc. 1899, 75, 20-36). Segundo palavras do próprio autor: "The red oil, is extremely active, and taken in doses of 0.05 g induces decided intoxication followed by sleep. The symptoms produced by it are peculiar to Cannabis indica, and as none of the other products appear to possess this action, this substance must be regarded as the active constituent of the plant."
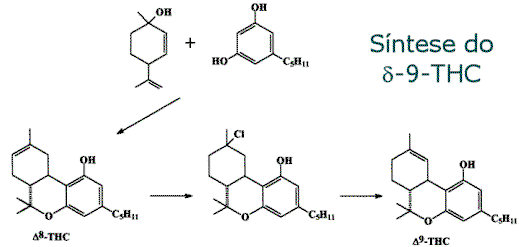
Como se chegou ao d-9-THC!
Em 1930, Cahn isolou o cannabinol - extraído a partir do óleo de Wood. Na época, acreditava-se que o cannabinol fosse o principal ingrediente ativo da cannabis. O químico americano Adams e o britânico Todd, na década de 1940, desenvolveram várias rotas sintéticas para análogos do cannabinol. Para sua surpresa, uma das rotas levou a um composto com intensa atividade biológica, muito maior do que o cannabinol. Era o d-9-THC (J. Amer. Chem. Soc. 1949, 71, 1624-1628). Dentre os vários derivados preparados, o d-9-THC era o mais ativo. Os químicos da época, então, desconfiaram que a cannabis deveria ter, também, este terpenóide. Entretanto, foi somente em 1964 que a primeira isolação do d-9-THC na forma pura ocorreu. Os químicos Gaoni and Mechoulam obtiveram, de uma extração com hexano de uma amostra de hashish, vários cannabinóides, entre ele o d-9-THC, na forma cristalina.
A Ciência não parou mais...
Maior até do que dos usuários, o interesse dos cientistas pela marijuana está sempre se renovando: todos ficam fascinados pelo poder que as substâncias contidas nesta planta exercem sobre o homem. Entretanto, foi somente em 1988 que a pesquisa sobre a maconha deu um grande salto: Howlett et al. (Mol. Pharmacol. 33, 297-302) descobriram a existência de neurorecpetores para os compostos cannabinóides: isto é, determinados grupos de proteínas existentes em alguns neurônios cujo objetivo era unicamente o de se ligar a compostos com estrutura química semelhante a dos cannabinóides. Howlett chamou estes receptores de CB1; em 1993, outro grupo de receptores para cannabinóides foi descoberto, desta vez por Munro et at. (Nature 1993;365:61). Munro chamou este novo grupo de receptores como CB2.
Diversas pesquisas, desde então, mostraram que os efeitos farmacológicos da marijuana são mediados por estes dois receptores. Ambos ativam mecanismos de transdução similares, incluindo a inibição da adenilate ciclase e de canais de Ca
2+
do tipo N. O CB1 ocorre no cérebro, onde é responsável por efeitos característicos da cannabis (relaxação, bem-estar, analgesia, aumento da percepção audio-visual, depressão da atividade motora, analgesia e catalapsia) e também no sistema nervoso periférico. Aí, os receptores CB1 são localizados pressinapticamente e sua ativação pode produzir uma supressão da liberação de neurotransmitores. Os principais sintomas da ativação destes receptores são a estimulação do apetite, vasodilatação (particularmente dos vasos conjuntivos), taquicardia e inibição da mobilidade instestinal.
Os receptores CB2, até agora, somente foram localizados fora do SNC (sistema nervoso central), principalmente em células do sistema imunológico. Muitos autores relacionam a ativação destes receptores com imunosupressão, efeitos anti-inflamatórios e analgesia associada a processos inflamatórios. Ao contrário dos receptores CB1, pouco se sabe, ainda, sobre este grupo de receptores.
Era quase inconcebível para a maior parte dos neurologistas que o cérebro animal fosse gastar parte de seus nutrientes e mecanismos simplesmente para elaborar um receptor para uma substância provinda de uma planta. Tal como com a morfina, a descoberta de receptores biológicos para cannabinóides exógenos levantou a possibilidade para a existência de cannabinóides endógenos. Muitos químicos e bioquímicos, então, focaram seus esforço no sentido de descobrir candidatos a ocupar esta posição: cannabinóides endógenos.
O primeiro ligante cannabinóide endógeno a ser isolado foi a etanolamida da arachidonila, chamada de anandamida. O nome vem da palavra "ananda", cujo significa em sânscrito é "prazer". Tão logo esta descoberta foi anunciada, centenas de veículos de comunicação publicaram manchetes como "Descoberta a molécula do prazer", ou "Cérebro produz maconha". Obviamente, um péssimo jornalismo científico, como sempre. Na verdade, a anandamida tem poucos efeitos similares ao THC, além de ser facilmente hidrolisada quando em contato com o receptor. Porém, várias situações estimulam o organismo a despejar grandes quantidades de anandamida nas fendas sinápticas: autores sugerem que esta droga esteja relacionada a momentos de relaxamento, prazer e calma. Um derivado sintético da anandamida - a metanandamida - possui uma potência mais elevada e maior estabilidade e mostrou-se portadora de grande efeito fisiológico. Outros derivados eicosanóides capazes de se ligarem aos receptores cannabinóides já foram isolados dos mais distintos tecidos humanos. Entre estes, o 2-arachidoniglicerol, considerado um dos mais potentes cannabinóides endógenos.